 Profi-Gärtner | Kulturdatenblätter | Die Düngung | CEC – pH - Leitfähigkeit
Profi-Gärtner | Kulturdatenblätter | Die Düngung | CEC – pH - Leitfähigkeit
Gießwasser und Düngung ergeben verschiedene Resultate je nach Reaktion des Substrates. Diese Reaktion wird durch die C.E.C (Kationenaustauschfähigkeit) und durch die Fixierfähigkeit beschrieben.
Die Resultate beziehen sich vor allem auf die pH-Werte und die Leitfähigkeit innerhalb des Substrates.
Durch ihre natürliche Beschaffenheit sind organische Stoffe und Ton negativ geladen: die Anionen. Die Kationen dagegen sind positiv geladene Moleküle.
Im Substrat gibt es zwei verschiedene Formen von Kationen:
Eine einfache Darstellung der Adsorption ist sehr ähnlich mit der Aktivität, die zwischen zwei Magneten gilt:
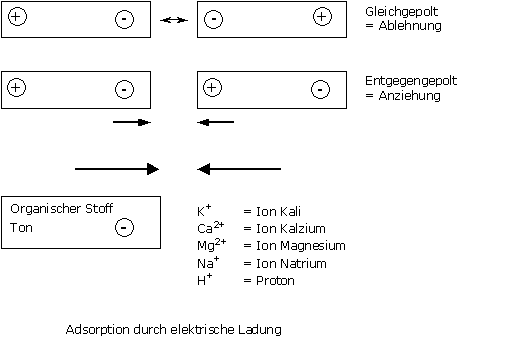
Die Anziehungskräfte zwischen den adsorbierten Kationen und der Oberfläche der organischen Stoffe oder Ton sind schwach. Diese Verbindungen können leicht unterbrochen werden.
Die dabei wirkenden Verbindungskräfte sind schwach. Dadurch erfolgt ein Daueraustausch zwischen der Substratlösung und den Adsorptionsorten.
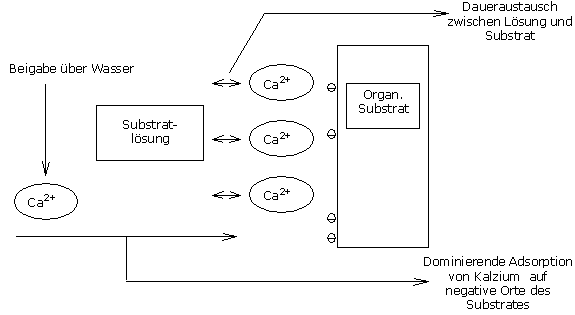
Sind im Substrat noch Stellen frei, führt die Beigabe von Kalziumionen zu einer Kalziumadsorption.
Bei einem pH-Wert von 5,5 ist die Kationenaustauschfähigkeit des Substrates nicht vollständig mit Kalzium gesättigt.
Die Kalziumionen des Wassers werden auf die freiverfügbaren negativ geladenen Stellen des Substrates adsorbiert, bis diese gesättigt sind.
Der Sättigungsgrad der Kationenaustauschfähigkeit wird erreicht. (CEC)
Wird der pH-Wert stabilisiert, wenn die Kationenaustauschfähigkeit mit Kalzium gesättigt ist?
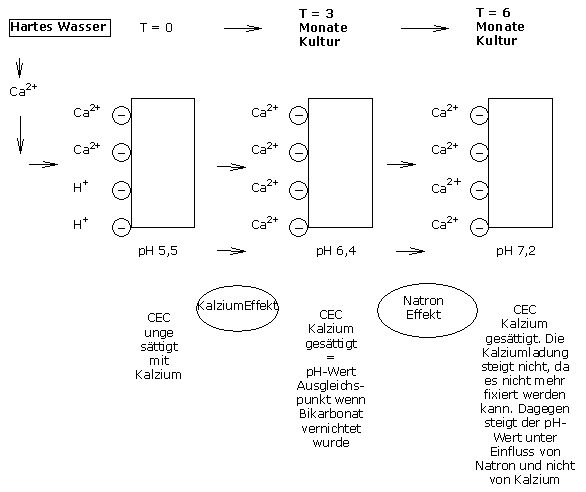
Wenn hartes Wasser in Zusammenhang mit einem « reaktiven » Substrat verwendet wird, erzeugt Kalzium die Stabilisierung des pH-Wertes der Kationenaustauschfähigkeit (CEC).
Wenn Bikarbonat (doppelsaures Natron) zerstört wird, bleibt die Kationenaustauschfähigkeit durch die Kalziumionen ständig gesättigt, was eine gute Stabilisierung des pH-Wertes innerhalb des Substrates bewirkt.
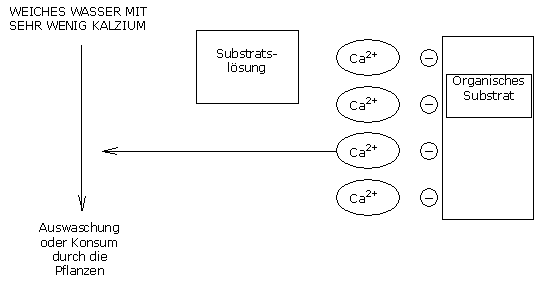
Das durch die Kationenaustauschfähigkeit der organischen Substrate festgesetzte Kalzium wird in der Substratslösung wieder verfügbar, so dass man immer einen identischen Ausgleich, zwischen der Kalziumladung in der Lösung und der Kalziumladung im Substrat, hat.
Die verlorenen Kalziumionen der Kationenaustauschfähigkeit werden durch H+ Ionen ersetzt (Protonen).
Diese H+ Ionen wirken säuernd und führen zu einer Abnahme des pH-Wertes.
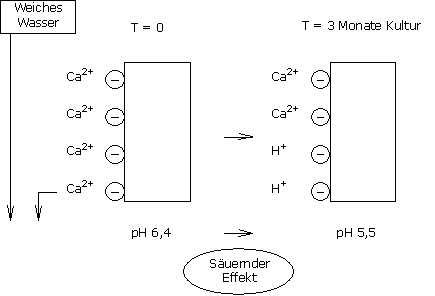

NB: Schwarztorf hat eine mindestens 3 mal höhere Pufferung als heller Torf.


Die auf CEC fixierte Mengen sind 40 mal höher als in der Lösung für Kalzium und 17 mal höher als Magnesium.
Kalzium- und Magnesiummängel in Substraten mit pH-Werten von höher als 5,5 sind nicht realistisch. Das Gleiche gilt für die schwach gepufferten Substrate mit großen CEC Reserven dieser Elemente.
« Nährstoffmangel », d.h. eine ungenügende Kalzium- und Magnesiumaufnahme in klassischen organischen Substraten, werden «induziert» durch eine Unausgeglichenheit der Faktoren Giessen: Substrat.
Beispiel der Kalziumnitratbeigabe in ein Substrat aus hellem Torf (wenig gepuffertes Substrat):
Bei einem pH-Wert von 5.5, schwacher pH-Wert, wird während 15 Tagen Kalziumnitrat (6 x 1 g./Liter) beigegeben.
Der Kalziumsättigungsgrad der CEC liegt dann bei 50%.
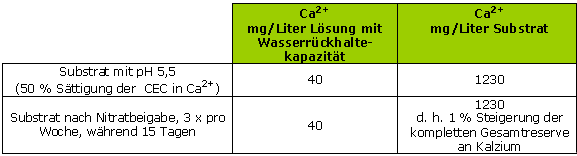
Dieses Beispiel zeigt, ohne Rücksicht auf das Substrat, die illusorische Seite einer schnellen Umkehr des pH-Wertes mit Kalzium-Nitrat.
Das Substrat hat einen Ausgangs pH-Wert von 5,5 ; d. h. 50 % Kalziumsättigung und 25 % Magnesiumsättigung.
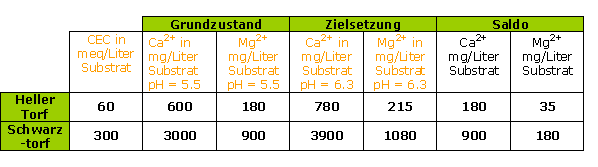
Hartes Wasser mit 80 meq/Liter Ca2+ (4 mg/Liter Ca2+) und 20 mg/Liter Mg2+ (1.7 meq/Liter Mg2+):
Ein mittlerer Gießvorgang von 100 ml/Liter Substrat bringt: 8 mg Ca2+ und 2 mg Mg2+
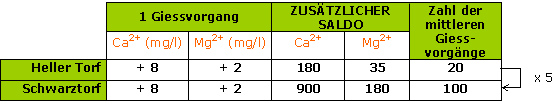
Um den pH-Wert um eine Einheit steigen zu lassen, muss mit hartem Wasser bei einem « schwarzen » Substrat durchschnittlich 4 bis 5 x mehr gegossen werden, als bei einem hellen Substrat.
Bei pH-Werten niedriger als 4.5, und daher für CEC dessen Sättigungsrate unter 30% Ca2+ und Mg2+, ist das Mangelrisiko real: Azaleen werden blau, einige Moorbeetpflanzen werden in ihrem Wachstum gehemmt.
Außer o.g. Extremfällen trifft man im Zierpflanzenbau meist auf Mängel, die auf ein schlechtes Verhältnis zwischen Substrat: Giessen zurückzuführen sind.
Das Magnesium wird um so schlechter angenommen, je länger und seltener die Gießphasen sind.
Eine unzureichende Belüftung der Wurzel führt auch zu Aufnahmeschwierigkeiten von Magnesium.
Je kräftiger die Sorte ist, um so schlechter wird Kalzium von Cyclamen angenommen.
Mangel von Ca oder Mg kann durch Gießen, senken der Luftfeuchtigkeit im Gewächshaus, sowie Veränderung der Tag/Nachttemperatur behoben werden.
Kali ist ein Kation mit dem schwächsten Fixierprozentsatz (zusammen mit Ammoniak) d. h. dass Kalireserven im Durchschnitt nur 2,5 % der CEC ausmachen.
Darüber hinaus wird die gleiche Menge Kali in der Lösung fixiert. Kali ist gegen „Auswaschen“ empfindlich.
In einem organischen Substrat wird Kali durchschnittlich 2 x langsamer ausgewaschen als Nitratstickstoff.
Zu beachten ist, dass Ammoniakionen fast den gleichen « Verspätungs »-Effekt wie Kali aufweisen (und dennoch redet man in diesem Fall von Reserven!).
Die Fixierfähigkeit eines Substrates entspricht seiner Fähigkeit, Anionen oder Spurenelemente zu fixieren.
Diese Fixierfähigkeit ist mit der Anwesenheit von kolloidalen, organischen Stoffen oder Ton, oder auch mit der Anwesenheit von Eisen oder Aluminium, verbunden.
Die Fixierfähigkeit von einigen Böden im Bereich Phosphor ist bekannt und mit der Anwesenheit von Kalk verbunden.
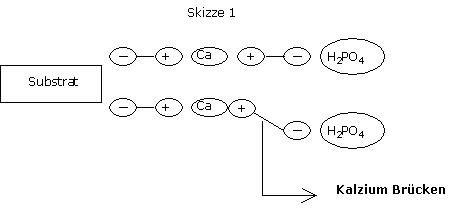
In den organischen Substraten liefern die Kalzium Brücken wenig Energie.
Fixierfähigkeit von Phosphor wird eher mit der Anwesenheit von Torfsorten, die an Aluminium oder an Eisen reich sind, verbunden.
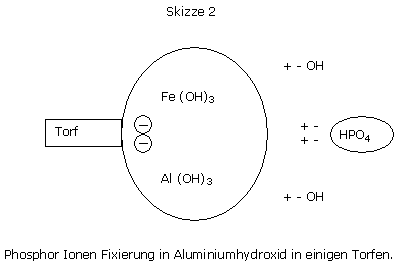
Die Fixierenergie des Phosphors auf Torf kann so hoch sein, dass Phosphate für Cyclamen nicht aufnehmbar sind.
Es ist notwendig, alle Stellen mit Aluminiumphosphaten zu durchtränken, so dass jede Phosphatbeigabe durch die Düngung aufnehmbar bleibt und daher wasserlöslich wird.
Das ist die Rolle der Grunddüngung.
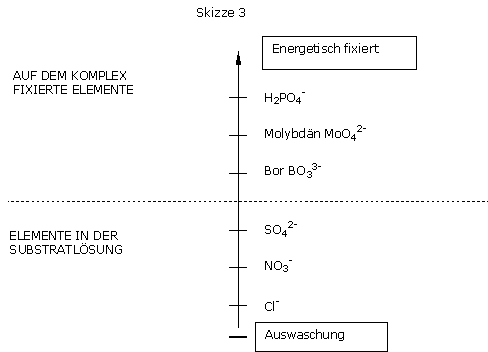
Cl-: Chloride und Nitratstickstoff sind absolut auswaschbar.
SO42-: Die Sulfate sind ebenfalls auswaschbar, haben aber die Eigenschaft, sich als Gyps-Mikrokristalle (CaSO4, 2H2O) abzusetzen. Diese Mikrokristalle häufen sich und senken für eine gewisse Zeit die Sulfat-Konzentration des Substrates. Am Ende einer langen Kultur wird die Trennung langsamer und der Sulfatgehalt kann steigen, wenn der „Wasserspülungs-Effekt“ nicht ausreicht.
Es ist darauf hinzuweisen, dass sulfathaltige Dünger eine stärkere übersalzende Wirkung haben, als ihre Äquivalente Nitrat oder Phosphat. Daher sollten sulfatarme Dünger ausgewählt werden, um die sofortige salzige Wirkung zu begrenzen.
BO33-: Bor wird im organischen Komplex adsorbiert. Sein Übergang in die flüssige Lösung ist schnell. Seine Aufnahmebereitschaft wird umso schlechter, je höher die Intervallfrequenz von reichhaltigen Gießphasen und Wasserstress ist.
Diese Situation ist typisch für den Sommer.
MoO42-: Molybdän wird als nicht auswaschbar betrachtet, außer in einem sauren pH-Wert.
Die vorherigen Spurenelemente sind im organischen Substrat hauptsächlich chelatiert anwesend: die Chelate schützen die Spurenelemente vor Auswaschung.
Spurenelemente sind wenig wasserlöslich.
Die Assimilation findet im Wesentlichen durch einen Kontakt zwischen der Wurzel und dem Substrat statt. Wenn dieser Kontakt ungenügend ist, findet die Assimilation nicht statt und die Mängelrisiken steigen.
Eine sehr starke Fixierung des Kupfers durch fermentierende Elemente kann zu starken Missbildungen führen.
Alle biochemischen Reaktionen – ob beim Menschen, beim Tier oder in der Pflanzenwelt, werden durch ihre Umwelt beeinflusst.
Einer der Hauptfaktoren, die ein gutes Wachstum beeinflussen, ist der pH-Wert des Substrates.
Selbst der Pflanzensaft der Cyclamen hat einen sortenspezifischen pH-Wert.
Der pH-Wert ist ein Grundelement in der Ernährungsführung, da er die Aufnahmebedingungen der mineralischen Elemente festlegt.
Der pH-Wert misst die Konzentration der Wasserstoffionen, H+, daher der Name Wasserstoffpotential (Potential Hydrogen).
Dieser Wert bestimmt den Säuregehalt oder die alkalische Kapazität des Substrates.
pH = - log [H3O+]

Die am häufigsten angewendeten Bezugswerte sind: 1:1.5 ; 1:2.5 die zukünftige europäische Methode schlägt ein Verhältnis von 1:5 vor.
Der pH-Wert reagiert sehr schnell auf den Sauerstoffgehalt des Auszuges: je CO2 gesättigter der Auszug ist, um so höher steigt der pH-Wert des Wassers.
Je höher der Salzgehalt des Substrates ist, um so tiefer sinkt der pH-Wert des Wassers.
Der Abstand zwischen dem pH-Wert des Wassers und dem pH-Wert KCI ist dann sehr gering. Die Anwesenheit von Salzen und Düngern, die schwache Säuren oder schwache Basen sind, puffert das Verhalten von Wasserstoff.

Der pH-Wert des Wassers gibt am besten die real herrschenden pH-Bedingungen des Wassers im Wurzelbereich wieder.
Daher wird für die Beobachtung und den Verlauf der Düngung diese Messung durch den Gärtner verwendet.
Die, mit dieser Methode errechneten pH-Werte bleiben Zwischenwerte zwischen pH-Wert H2O und pH-Wert KCl.
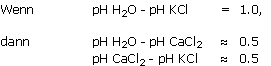
Diese aus dem Bodenbereich stammende Methode, besteht daraus, einen 1:2,5er Auszug mit einer KCl 1 N-Lösung.
Dieser pH-Wert zeigt den Sättigungsgrad der CEC und ist ziemlich unabhängig von den Substratbedingungen.
Dieser Wert erlaubt dann die Entwicklung des Sättigungsgrades oder der Entsättigung des Substrates in Ca und Mg.
Beispiel:
Messung in einer Zeit T der Kultur:
15 Tage später, durch entsprechende Gießvorgänge sinkt die Leitfähigkeit:
Der pH-Wert KCl bedeutet immer ein höherer Sättigungsgrad der CEC. Dieser pH-Wert übernimmt einen kohärenten Wert von 6.9, was ein Risiko für die Kultur bedeutet.

Die schlechte Steuerung des pH-Wertes ist ein ständig Risikofaktor in der Cyclamenkultur.
Die Aluminiumvergiftung als auch eine Manganvergiftung hängen mit einem saueren pH-Wert und instabilen, fermentierenden Stoffen zusammen.
Die Fermentierung verstärkt die Mangan- und Aluminiumreduzierung. Formen die dann wasserlöslich und potentiell toxisch werden. Dies verstärkt ein Ersticken der Wurzel (Sauerstoffmangel verbunden mit Fermentierung).
Dieses Vergiftungsphänomen ist häufig anzutreffen, wenn die pH-Werte während der Kultur sinken und die Leitfähigkeit zunimmt.
Molybdänmangel mit saurem pH-Wert ist seltener.
Bei höherem pH-Wert fällt die schlechte Verfügbarkeit des Phosphors kaum auf. Festzustellen ist ein schwaches Pflanzenergebnis.
Liegt der pH-Wert hoch, um etwa 7.1 bis 7.2, ist Bormangel vorhanden. Dieser Mangel wird oft im Sommer beobachtet. Bor ist nicht nur in diesem Messbereich wenig verfügbar, kommt eine unzureichende Wasserbeigabe hinzu, – wie häufig bei Cyclamen – wird die Boraufnahme zusätzlich behindert.
Bei hohem pH-Wert sind Eisenmangel und Manganmangel klassische Fälle bei den Sorten, die gegen Eisenchlorose empfindlich sind, zu welchen Cyclamen zählen. Als Knollenpflanzen nehmen Cyclamen diese beiden Elemente schlecht auf.
Vorsicht! Der pH-Wert des Wassers gibt keine Auskünfte über die Wasserhärte und über ihre Wirkung auf das Substrat.
Beispiel: Regenwasser
Regenwasser enthält kein Bikarbonat.
Es ist daher nicht gepuffert.
Dieses Wasser übernimmt den pH-Wert des Substrats durch welches es fließt.
Im Auffangbecken gelagert, erreicht der pH-Wert oft Werte nahe von 8,0! In diesem Fall bezieht sich der pH-Wert auf die Ladung der im Wasser gelösten Gase (speziell CO2).
Gegossen auf ein Substrat mit einem pH-Wert von 5,8 übernimmt Regenwasser diesen pH-Wert und führt allmählich zu einer Entkalzifizierung des Substrates und daher zu dessen Versäuerung.
Die « Härte » des Gießwassers hängt vom Gehalt an Bikarbonat HCO3- und nicht von seinem pH-Wert ab.
Die Bikarbonate bilden eine starke Base (das Gegenteil von einer starken Säure) da sie den pH-Wert stark ansteigen lassen.
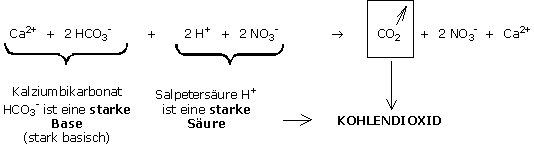
Die Bikarbonate verschwinden in Form von Kohlendioxid und bleiben ausgeglichen als schwache Säure / schwache Base: NO3-:Ca2+ in der Lösung.
Der pH-Wert kann daher nicht mehr steigen.
Dieser Wert ist stabil, da das immer anwesende Kalzium im Wasser die Ca2+ Verluste in der CEC ausgleicht.
Weiches Wasser enthält keine Bikarbonate
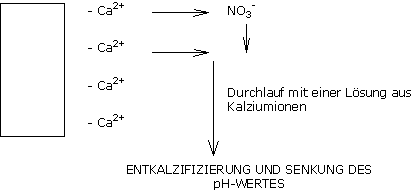
Um die Kalziumverluste auszugleichen und den pH-Wert zu stabilisieren, ist eine Ergänzung mit Kalziumnitrat notwendig.
Säurebildende Eigenschaften der Dünger stammen aus Ammoniakkomponenten.
Die Dünger enthalten Harnstoffe und einige Langzeitdünger (in der Cyclamenkultur nicht empfohlen), die mit Harnstoffpolymeren säurebildend wirken, da durch Hydrolyse die Harnstoffe zu Ammoniakstickstoff werden.
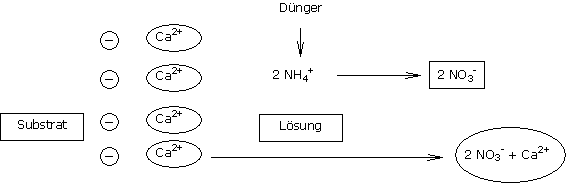
Die Umwandlung von Ammoniakstickstoff in flüssigen Nitratstickstoff führt dazu, dass ein Kation Ca2+ (oder Mg2+) auf der CEC fixiert in die Lösung wechselt, um diese elektrisch auszugleichen.
Die Lösung von Kalziumionen und Mangnesiumionen begünstigen die Vergiftung des Substrates.
Manche Dünger beinhalten starke Säure die ein Teil der vorhandenen Bikarbonate zerstören.
pH-Wert und biologische Stabilität der anwesenden organischen Stoffe.
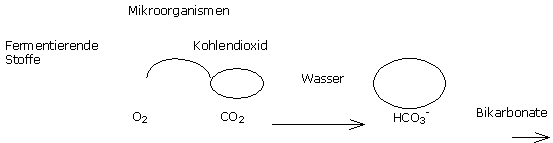
Die Fermentierung von frischer Rinde und Kompost führt zur Produktion von Kohlendioxid in der Substratlösung.
Ein starker Kohlendioxiddruck im Wasser fördert die Bildung von Bikarbonaten und erhöht den pH-Wert.
Am Ende einer 6 Monate Kultur kann eine Rindenmischung, die am Anfang einen pH-Wert von 5.8 hatte, pH-Werte von über 7.2 aufweisen.
Gramm / Liter drückt aus, wie hoch der Salzgehalt in der Substratlösung ist.
Es wird mittels der elektrischen Leitfähigkeit gemessen.
Die Messung basiert auf der Eigenschaft der Elektrolyte (Substanzen zerfallen in Ionen nach ihrer Auflösung), den elektrischen Strom umso leichter zu führen je höher die Salzkonzentration ist.
Es existieren zwei Ausdrucksweisen:
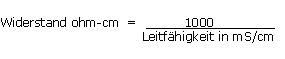
Das Messen der Leitfähigkeit wird in Frankreich oftmals auf einem Auszug von 1:1,5 durchgeführt:
1 Substratvolumen zu 1,5 Volumen demineralisierten Wasser.
Die Messung wird mit der empfohlenen Filtrierung nach einem Kontakt von mind. 20 Minuten Dauer durchgeführt.
Der direkte Effekt des Salzgehaltes der Substratlösung besteht darin, einen osmotischen Druck herzustellen, sodass die Cyclame kein Wasser mehr aufnehmen kann. Dies bezeichnet man als physiologische Trockenheit (Dürre).
Dieses Verfahren wird für die Steuerung der Wachskraft angewendet.
Die Wuchskraft einer Knollenpflanze hängt vor allem mit einer „Regelmäßigkeit“ der Produktionsfaktoren zusammen. Je regelmäßiger die Gießphasen und die konstante Leitfähigkeit sind, desto besser Wuchskraft und vegetative Gleichgewicht.
Bei blühenden standard Topfcyclamen ist die Leitfähigkeit eher niedrig.
Im Fall von Mini-Cyclamen und bei Substraten mit hohem Torfanteil (d. h. mit einem schwachen realen Salzgehaltskoeffizient), erhöhen sich die Leitfähigkeitswerte und sorgen für einen kompakten Pflanzenhabitus. Der Gießrhythmus auf schwachen Substratvolumen fordert einen Wasserkomfort, der auf höhere Leitfähigkeit kontrolliert werden soll.
Die Messung der Leitfähigkeit kann dazu verwendet werden die Ernährungsgrenze des Substrates zu testen.
Beispiel 1:
Extraktion 1:1,5 vol. Messung der Leitfähigkeit und der Spurenelemente auf ein mit PG Mix 1 kg/m3 bereichertes torfhaltiges Substrat
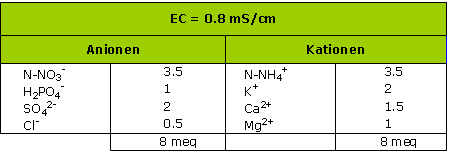
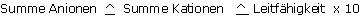
In diesem Beispiel kann die Messung der Leitfähigkeit die stickstoffhaltige Fraktion unterschätzen.
Tatsächlich wird Ammoniakstickstoff nitrifiziert und die Leitfähigkeit steigert sich schematisch um den selben Wert.
Beispiel 2:
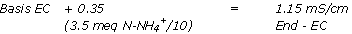
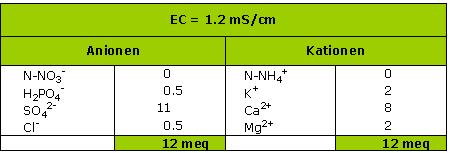
Der gemessene Leitfähigkeitswert gibt zuerst einen annehmbaren Nährwert an, obwohl die Leitfähigkeit nur mit einer hohen sulfathaltigen Charge verbunden ist (die organische Stoffe produzieren Sulfate während ihres Reifeprozesses).
Empfehlenswert ist, eine Stickstoffmessung mit schnellen Tests z. B., aus diesem Extrakt durchzuführen.
Vorsicht bei einem Salzüberschuss! Er führt zu einer Überempfindlichkeit gegen Krankheiten, einer Schädigung der adsorbierenden Wurzelhaare und einer schlechten Verteilung von Kalzium und besonders Magnesium.
2565, rue de Montourey
83600 Fréjus - France
International : +33 (0)4 94 19 73 04
Tel : + 33 (0)4 94 19 73 00
Fax : +33 (0)4 94 19 73 19

